日本では、2020 年にがんに罹患した人が 100 万人を超えました。特に、肺がん、胃がん、前立腺がん、大腸がん、乳がんが最も多くなっています*1。「Guardant360® CDx」は、腫瘍が血液中に滲出する血中循環腫瘍 DNA (ctDNA) を次世代シークエンサーによって解析するがん遺伝子パネル検査として、2022 年 3 月 10 日に厚生労働省より承認されました。固形がん患者さんの血液検体からがん細胞由来のctDNA を検出し、がんに関連する 74 の遺伝子を網羅的に調べます。本検査は、国内で承認された複数のがん治療薬に対するコンパニオン診断機能を併せ持ち、包括的ながんプロファイリング結果を提供します。
「Guardant360® CDx」は、ペムブロリズマブによる治療効果が期待されるマイクロサテライト不安定性高値(MSI-High)固形がん患者さんならびにニボルマブによる治療効果が期待される MSI-High 進行大腸がん患者さんを特定するコンパニオン診断として、厚生労働省により承認されています。また、ソトラシブによる治療効果が期待される転移性非小細胞肺がん患者さんを特定するコンパニオン診断としても厚生労働省から承認されています。
当社の代表取締役社長 浅野 元は、「本日より、Guardant360® CDx がん遺伝子パネルの販売が開始されることを大変うれしく思います。本検査の提供により、進行・再発のがん患者さんの固形腫瘍を検体とした検査が実施困難な場合でも、有意義な治療結果に繋がり得る情報提供が可能となります。当社のミッションは“データを駆使してがん克服に貢献すること”です。CGP の普及を通じ、がん治療における個別化医療のさらなる高度化と、患者さんの治療結果の向上を目指して、全力で取り組んでまいります」と述べています。
「Guardant360® CDx」は、2020 年8月に米国FDA の承認を受け、2021 年3月には EU においてCE マーク*2 が付与されています。全血検体を用いた包括的なゲノムプロファイリング検査として広く採用され、350 件以上の査読付き論文が出版されています。これまでに、世界で 12,000 人以上の医師により、400,000 件以上の検査が実施されています。
References:
1. International Agency for Research on Cancer. Japan. Globocan 2020. Accessed online June 29, 2023. htps://gco.iarc.fr/today/data/factsheets/populations/392-japan-fact-sheets.pdf
2. EU 加盟国の法律で定められた安全性能基準を満たす製品に付与される基準適合マーク
製品情報
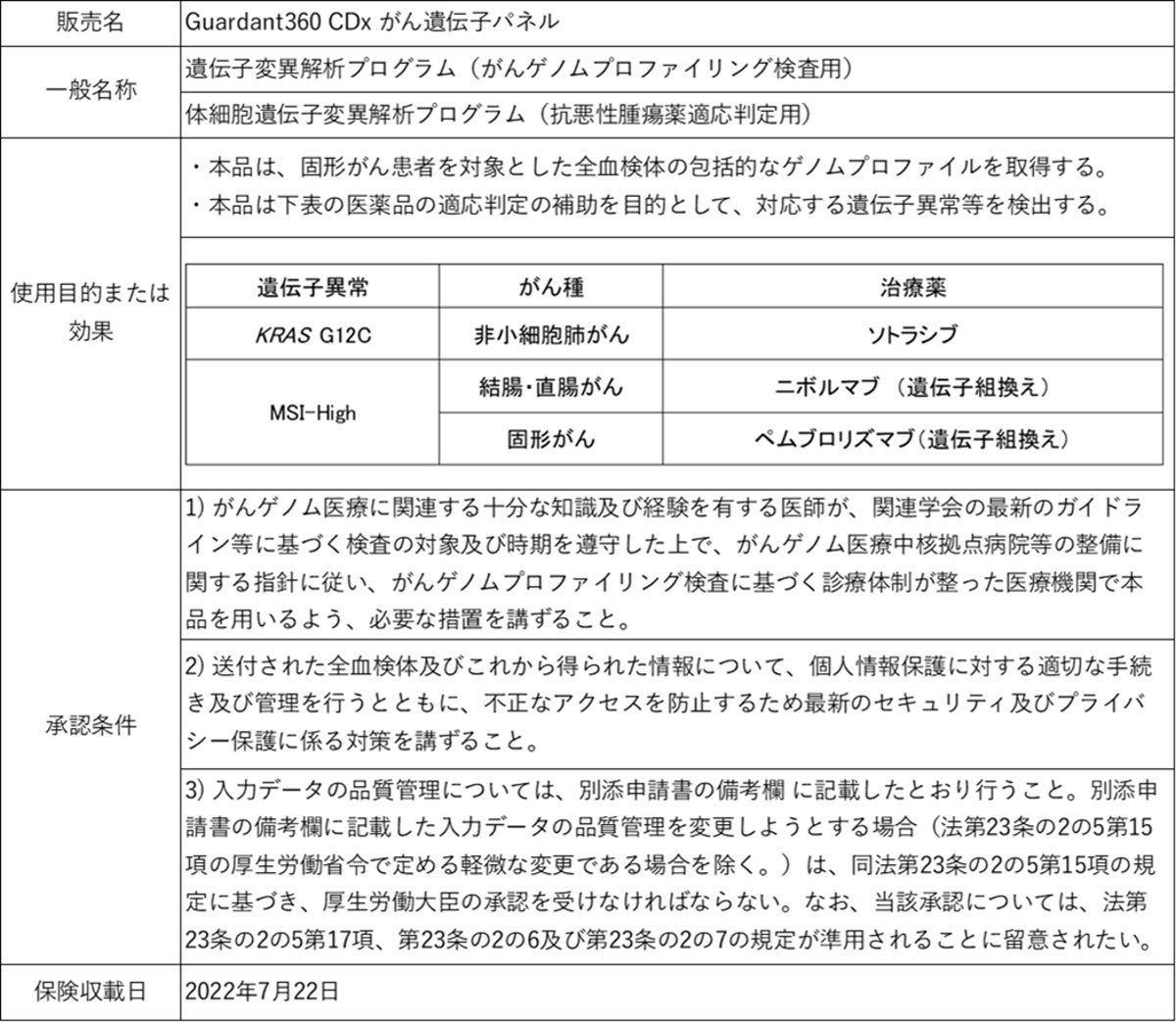
ガーダントヘルスジャパン株式会社について
ガーダントヘルスジャパン株式会社は、アジア、中東、アフリカにおいて事業展開する Guardant Health Asia, Middle East & Africa, Inc(Guardant Health AMEA)の日本子会社です。リキッドバイオプシー(液体生検)検査から、がんの遺伝子異常を検出する、独自の最先端技術、蓄積された膨大なデータ、高度な解析力により、がん克服に貢献することを目指しています。当社のがん治療プラットフォームは、技術、臨床開発、薬事規制、保険適用に関する知識を集結し、治療領域における普及、患者さんの臨床アウトカムの改善、医療費削減を推進するように設計されています。ガーダントヘルスジャパン株式会社の詳細は、https://guardanthealthjapan.com をご覧ください。
株式会社エスアールエルについて
日本有数のヘルスケアグループであるH.U.グループの一員である SRL は、1970 年の設立以降、国内最大の検査ラボラトリーとして総合的なテストサービスを提供しております。SRL は年間で 4 億件近い検査を行っており、その検査サービスは、一般・緊急検査、特殊・研究用検査、コンパニオン診断やゲノム診断といった幅広い分野をカバーしております。
より詳細な情報は、SRL ホームページ https://www.srl-group.co.jp/をご覧ください。
Guardant360® CDx について
「Guardant360® CDx」は、腫瘍が血液中に滲出する血中循環腫瘍 DNA (ctDNA) を次世代シークエンサーによって解析するがん遺伝子パネル検査です。この検査は、がん患者さんから採血した全血検体を用いて包括的なゲノム情報を提供することで、医師が患者さんに最適化された個別化医療を届けるために必要な情報を、適時に速やかに得られるよう支援しています。米国において自家調製検査(Laboratory Developed Test: LDT) として導入されて以降、「Guardant360® CDx」 は、全血検体を用いた包括的なゲノムプロファイリング検査として広く採用され、350 件以上の査読付き論文が出版されています。これまでに、世界で 12,000 人以上の医師により、400,000 件以上の検査が実施されています。
ガーダントヘルスの将来予想に関する声明
本プレスリリースは、ガーダントヘルスのリキッドバイオプシー、または分析の潜在的な効用、価 値、利益および利点に関する声明などの米国連邦証券法の意味での将来予想に関する声明を含みま す。これらの検査、または分析には、実際の結果をこれらの将来予想に関する声明に記載された予期される結果および予想とは大きく異なる可能性があるリスクおよび不確実性が伴います。これらの声明は、現在の予想、予測および想定に基づくもので、実際の成果および結果は、複数の要素が原因でこれらの声明とは大きく異なる可能性があります。ガーダントヘルスの財務成績および運用実績に影響を与える可能性がある、ならびに実際の結果を、本プレスリリースで行われる将来予想に関する声明が示すものとは大きく異なる可能性があるこれらのおよび追加的なリスクおよび不確実性は、昨年度に関するフォーム 10-K 上のガーダントヘルスの年次報告において「リスク要素」および「マネジメントによる財務状況および営業実績の議論および分析」の見出しの下などで議論されたもの、ならびに米国証券取引委員会に届け出られたガーダントヘルスのその他の報告で議論されたものを含みます。本プレスリリースに含まれる将来予想に関する声明は、その日付においてガーダントヘルスが入手可能な情報に基づくものです。ガーダントヘルスは、法的に必要な場合を除き、ガーダントヘルスの予想の変化、または当該声明の基礎となる事象、条件もしくは状況の変化を反映するよう提供済みの将来予想に関する声明を更新する義務を否定します。本プレスリリースの日付以降のいかなる日付においても、ガーダントヘルスの見解を示すものとしてこれらの将来予想に関する声明に依拠すべきではありません。


