
本検証で活用した技術は、2021年7月から9月にかけて実施した「Toshiba OPEN INNOVATION PROGRAM 2021」(注5)において、Revorfおよびアヘッド・バイオコンピューティング株式会社と実施した「組合せ最適化ソルバーを活用した創薬ソリューションの検討」の成果(注6)を発展させて開発したものです。
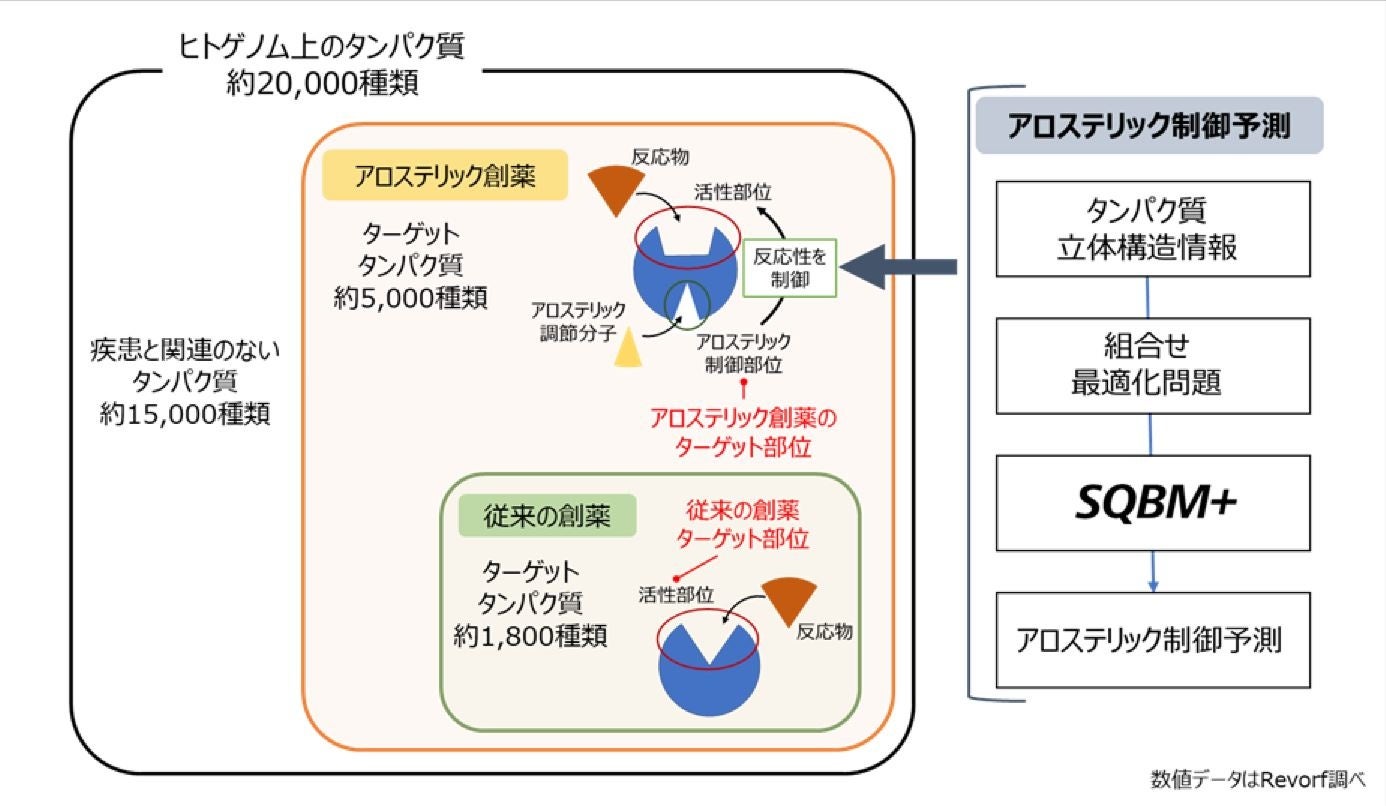
昨今、創薬プロセスにおいて、創薬ターゲット(注7)の枯渇が課題になっています。これに対して、アロステリック制御に着目した創薬手法(アロステリック創薬)では、従来、創薬困難とされていたタンパク質(undruggable target)を創薬ターゲット候補(druggable target)として見出すことが可能であり、ターゲットの枯渇という創薬課題の解決に期待が寄せられています。タンパク質におけるアロステリック制御部位(注8)を発見するためには、多大な労力と時間を要する in vitro実験が必要であることから、これを計算によって代替する技術が求められていました。
東芝デジタルソリューションズのSQBM+は、株式会社東芝 研究開発センターにおける量子コンピューターの研究過程で発明されたシミュレーテッド分岐アルゴリズムを実装した組合せ最適化問題を高速に求解するソリューションで、計算量が膨大で従来のコンピューターでは解くことができなかった問題において最適解を見つけ出すことができます。本検証では、アロステリック制御の予測をSQBM+が得意とする組合せ最適化問題として解く新たな技術を東芝デジタルソリューションズとRevorfが共同で開発し、従来手法の計算で特定できていなかったアロステリック制御部位を計算で予測することに成功しました。
本検証ではKRAS(注9)を含む複数のタンパク質に対して、SQBM+で計算し予測したアロステリック制御部位と、既知のアロステリック制御部位を比較し、従来の計算手法では特定できていなかった部位を、SQBM+による計算でより正確に予測できていることを確認しました。これによって、計算のみでアロステリック制御部位を発見でき、創薬候補化合物の探索を加速できる可能性が高まります。
計算によるアロステリック制御の予測
本検証で開発した技術はタンパク質の立体構造情報をもとに、タンパク質のアロステリック制御機構をSQBM+が得意とする組合せ最適化問題として定式化し、計算によってアロステリック制御を予測します。近年、クライオ電子顕微鏡(注10)によるタンパク質立体構造の決定やAlphaFold2(注11)などのAIによるタンパク質立体構造の予測など、タンパク質立体構造解析技術の飛躍的な躍進が報告されており、それに伴い多種多様なタンパク質の立体構造情報が急速に蓄積されてきています。今後、このタンパク質立体構造情報というビッグデータをもとにアロステリック制御を予測することが可能になることから、新たなアロステリック創薬手法として、新薬開発の加速と成功確率の向上が期待できます。
株式会社Revorfの代表取締役である末田伸一は、「Revorfは、遺伝子情報やタンパク質情報などの生命情報を解析、応用することで、人々の健康に貢献致します。未だ有効な治療薬が存在しない疾患が多数あり、多くの患者様が苦しんでいます。本技術により、創薬可能な新規ターゲット領域を検出することで、創薬ターゲットの枯渇により有効な治療薬の創出が困難であるという課題の解決を目指します」と述べています。
東芝デジタルソリューションズ株式会社の取締役社長である岡田俊輔は、「東芝デジタルソリューションズは、量子インスパイアード最適化ソリューションSQBM+を社会のさまざまな課題に適用し、さまざまな領域で複雑化する社会課題の解決に貢献していきます。今回、SQBM+により、創薬における課題であった創薬候補の枯渇を解決する技術への貢献を目指し、検証を行いました。今後は、さまざまな創薬の場面でSQBM+を活用することで、新薬開発の革新に貢献していきたいと考えています」と述べています。
Revorfは、本検証によって得られた技術とRevorfの有するタンパク質機能解析技術を組合せ、新たな創薬ソリューションを提供します。
東芝デジタルソリューションズは、本検証を含むSQBM+を創薬分野に広く活用してもらうことで、医療分野における社会問題の解決に貢献していきます。
■株式会社Revorfについて
Revorf は、独自のRNA等遺伝子検出解析技術やタンパク質情報解析技術、データ分析・AI 技術とを掛け合わせ、新しい医療技術・創薬基盤手法の確立を目指しております。
注1:東芝デジタルソリューションズプレスリリース(2022年3月):量子インスパイアード最適化ソリューション「SQBM+™」の提供開始について:https://www.global.toshiba/jp/company/digitalsolution/news/2022/0302-2.html
注2:タンパク質は必要なときに適宜機能を発揮するように調節因子により制御されており、この機構をアロステリック制御という。調節因子が結合する部位(アロステリック制御部位)を標的にすることで、創薬ターゲットの増大、特異性の高い薬剤の創出、さらに副作用低減の可能性など多くの利点があるため、アロステリック制御部位を同定する技術は新薬開発の成功確率を高めるカギとなる技術と考えられている。
注3:計算創薬:計算科学を利用して薬をつくる創薬手法。
注4:in vitro実験:in vitroとは「試験管内で」という意味であり、in vitro実験とは、試験管や培養器内で生体内を模倣した環境を人工的に作り実験を行うことをいう。
注5:東芝プレスリリース(2021年7月):「Toshiba OPEN INNOVATION PROGRAM 2021」参加企業8社と協業検討を開始し、プログラムが本格スタート:https://www.global.toshiba/jp/news/corporate/2021/07/news-20210719-01.html
注6:東芝プレスリリース(2021年9月):「Toshiba OPEN INNOVATION PROGRAM 2021」成果発表会を開催:https://www.global.toshiba/jp/news/corporate/2021/09/news-20210927-01.html
注7:創薬ターゲット:疾患の責任分子と想定されるもので、治療薬をデザインする際に標的とするタンパク質
注8:アロステリック制御部位:タンパク質の活性中心以外の部位で、制御分子(アロステリック因子)が結合する領域
注9:KRAS:がん遺伝子のひとつ
注10:クライオ電子顕微鏡:液体窒素冷却下でタンパク質などの生体分子を観察することができる透過型電子顕微鏡。タンパク質の立体構造を高解像度で観察することが可能である。
注11:AlphaFold2:DeepMind社が開発したアミノ酸配列からタンパク質の立体構造を解析するAIシステム。
*SQBM+は、東芝デジタルソリューションズ株式会社の日本またはその他の国における登録商標または商標です。
*その他、本文章に記載されている社名および商品名はそれぞれ各社が商標または登録商標として使用している場合があります。
*ニュースリリース/トピックスに掲載されている情報(サービスの内容/価格/仕様/関連リンク/お問い合わせ先など)は、
発表日現在の情報です。予告なしに変更されることがありますので、あらかじめご了承ください。
■量子インスパイアード最適化ソリューション 「SQBM+」(日本語サイト)
https://www.global.toshiba/jp/products-solutions/ai-iot/sbm.html
株式会社Revorf
HP:https://www.revorf.jp/
本件に関するお問い合わせ先:information@revorf.com


